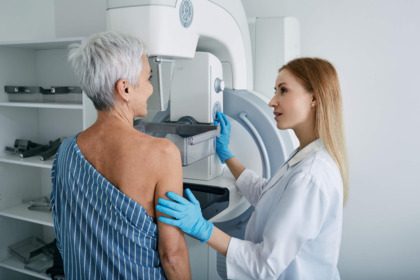
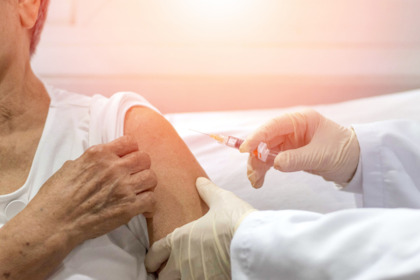
La sperimentazione di fase 1 ha confermato sicurezza e efficacia del vaccino a Rna anti-Coronavirus sviluppato dalla biotech Moderna. I dati definitivi entro l'autunno
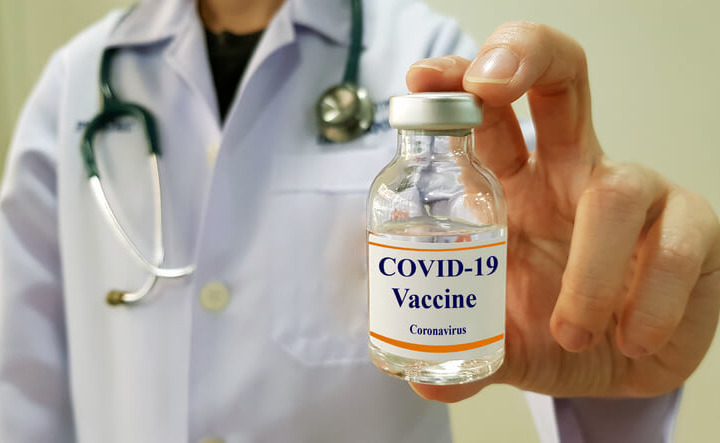
Sicuro e promettente, quanto a efficacia. Le prime evidenze riguardanti un possibile vaccino contro il Sars-CoV-2 - l’agente responsabile della malattia Covid-19 - riguardano l’antidoto a cui stanno lavorando i ricercatori dell’Istituto Statunitense per le Allergie e le Malattie Infettive (NIAID) e della società di biotecnologia Moderna. mRNA-1273, questo il nome dato al potenziale vaccino, è risultato infatti ben tollerato e in grado di innescare la produzione di anticorpi neutralizzanti in un gruppo di 45 persone adulte (18-55 anni) che hanno partecipato alla prima fase di sperimentazione. A raccontare l'esito di questo step iniziale della sperimentazione clinica è uno studio pubblicato sulle colonne del New England Journal of Medicine.
COME FUNZIONA IL VACCINO A RNA?
Il lavoro descrive le evidenze preliminari emerse dalla sperimentazione clinica di mRNA-1273, condotta arruolando persone sane attraverso il Kaiser Permanente Washington Health Research Institute di Seattle e la facoltà di medicina della Emory University di Atlanta. Il candidato vaccino è stato testato in due dosi, somministrate a distanza di 28 giorni l’una dall’altra: tra il 16 marzo e il 14 aprile scorsi. I partecipanti allo studio - nessuno dei quali si era già ammalato di Covid-19 - sono stati divisi in tre gruppi. Obiettivo: valutare la risposta a tre diversi dosaggi dell’antidoto (25, 100 o 250 microgrammi), iniettato per via intramuscolare nel deltoide. Andando a saggiare la presenza di anticorpi nelle persone sottoposte alla doppia dose vaccinale, ritenuta necessaria per registrare l’effetto neutralizzante a carico del virus, i ricercatori hanno rilevato «valori medi superiori a quelli misurabili nel siero delle persone che si sono ammalate di Covid-19 e che sono convalescenti»: questa la considerazione emersa dal confronto effettuato con gli anticorpi rilevati in 41 persone reduci dall’infezione.
CHE COSA SONO I CORONAVIRUS?
COME FUNZIONA mRNA-1273?
Il meccanismo d'azione di questo possibile antidoto al Sars-CoV-2 è diverso rispetto a quello della maggior parte dei vaccini. Il metodo più tradizionale prevede l'inserimento all'interno di una cellula di un virus innocuo (o di un antigene virale) in modo da simulare un contatto con l’agente infettivo e innescare una risposta immunologica simile a quella determinata dall’infezione naturale (senza che ciò arrivi però a causare la malattia e le sue complicanze). Attraverso il completamento della sintesi proteica, l'mRNA-1273 fornito dall'esterno mira invece ad aumentare la produzione di anticorpi in grado di neutralizzare le proteine «Spike», i grimaldelli posti sulla superficie del Sars CoV-2 che permettono al virus di legarsi ai recettori di membrana (ACE2) e di avviare la fusione con la membrana cellulare. Da qui l’ingresso dell’Rna virale che dà il la all’infezione. In questi cinque mesi si è osservato che, senza il contributo delle «Spike», il coronavirus non riesce a farsi largo nelle cellule bersaglio: localizzate perlopiù nei polmoni, ma anche (con certezza) nel naso e nell’intestino. Nel corso della sperimentazione clinica, i ricercatori hanno osservato un aumento degli anticorpi nelle due settimane successive alle somministrazioni. Un dato che denota una «risposta dose dipendente», come l’hanno definita gli autori dello studio, registrando il valore degli anticorpi presenti fino a quasi due mesi dopo l'avvio della profilassi.
Covid-19: il ruolo di plasma, anticorpi monoclonali e vaccini
GLI EFFETTI COLLATERALI RILEVATI
Al di là di una prima valutazione d’efficacia, gli studi di fase 1 puntano però a registrare la sicurezza di un farmaco. Il responso, anche in questo caso, è stato incoraggiante. Più della metà dei partecipanti allo studio ha registrato effetti collaterali quali l’affaticamento, il mal di testa, la comparsa di dolori muscolari e nel sito di iniezione. Nulla di più grave, però: da qui il moderato ottimismo dei ricercatori. I benefici, considerando la pandemia in atto, sono infatti stati considerati di gran lunga superiore ai rischi rilevati. Soltanto un paziente inserito nel primo gruppo (25 migrogrammi) è uscito dallo studio in corso d’opera, dopo aver sviluppato un’orticaria transitoria conseguente alla prima dose vaccinale. In linea generale, un maggior tasso di reazioni al vaccino è stato registrato nel terzo gruppo (250 microgrammi) dopo la seconda dose.
I PROSSIMI PASSI
L’avvio della sperimentazione di mRNA-1273 appare promettente, se si considera peraltro il drastico abbattimento registrato nei tempi di sviluppo. Un iter che di norma richiede diversi anni è stato in questo caso completato in due mesi: 66 i giorni trascorsi dal primo sequenziamento del genoma di Sars-CoV-2 all’iniezione del vaccino al primo paziente. Ora, anche al fine di capire la durata di questa protezione, lo studio andrà avanti. La fase 2 è già partita, con l’arruolamento di persone di età superiore a 55 anni. Ma il momento più atteso giungerà a partire da agosto, con il lancio dell’ultimo step della sperimentazione clinica. L’obiettivo è arruolare almeno trentamila persone in tempi brevi, così da poter avere i risultati già entro l’autunno. Quanto al dosaggio del vaccino, quello da 100 microgrammi sembra in grado di poter determinare il massimo beneficio a fronte di effetti collaterali gestibili e transitori.
Non fermare la ricerca. Dona ora per i pazienti più fragili.
Fonti

Fabio Di Todaro
Giornalista professionista, lavora come redattore per la Fondazione Umberto Veronesi dal 2013. Laureato all’Università Statale di Milano in scienze biologiche, con indirizzo biologia della nutrizione, è in possesso di un master in giornalismo a stampa, radiotelevisivo e multimediale (Università Cattolica). Messe alle spalle alcune esperienze radiotelevisive, attualmente collabora anche con diverse testate nazionali ed è membro dell'Unione Giornalisti Italiani Scientifici (Ugis).