Via libera da parte di Aifa alla commercializzazione e rimborso della Car-T Kymriah. Ora anche in Italia si potrà accedere a questa innovativa tecnica
Via libera a alla Car-T Kymriah. Aifa, l'Agenzia Italiana del Farmaco, ha dato parere positivo alla commercializzazione -e relativo rimborso- del trattamento in questione. A partire da settembre, in Italia, i pazienti che ne avranno bisogno potranno accedere alla cura Car-T. Un'ottima notizia se si pensa che sino ad oggi l'unica via per accedervi era all'interno di una sperimentazione clinica o tramite uso compassionevole.
CHE COSA SONO LE CAR-T?
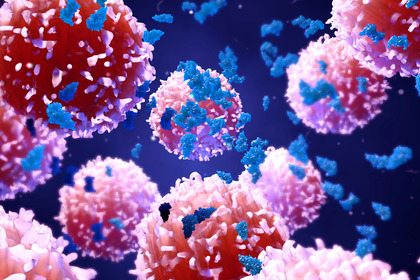
Da qualche tempo a questa parte, complice lo sviluppo di tecniche di manipolazione del Dna sempre più precise, gli scienziati sono in grado di agire sul "libretto di istruzioni" delle cellule immunitarie. Attraverso la terapia genica è infatti possibile veicolare dei frammenti di Dna all'interno dei linfociti in modo da insegnare loro a riconoscere il tumore. Nel caso delle Car-T le cellule del malato vengono prelevate, modificate in modo che esprimano Car -un recettore posto sulla superficie dei linfociti capace di aumentare la risposta immunitaria- e successivamente reintrodotte nel malato.
COME FUNZIONA?
La tecnica consiste nel prelievo dei linfociti T del malato per poterli così modificare geneticamente in modo tale che sulla loro superficie esprimano un particolare recettore chiamato Car (Chimeric Antigenic Receptor). La presenza di Car ha come effetto un potenziamento dei linfociti che li rende in grado, una volta reinfusi nel malato, di riconoscere e attaccare le cellule tumorali presenti nel sangue e nel midollo fino ad eliminarle completamente.
QUANDO SI UTILIZZA?
Al momento l’approccio si è dimostrato efficace per alcuni tumori del sangue e per un limitato numero di pazienti attentamente selezionati. Pur essendo terapie salvavita da utilizzare solo ed esclusivamente quando non si hanno più altre armi a disposizione, ciò non significa che per tutte le persone affette da questi tumori le Car-T siano indicate. Dall’agosto dello scorso anno l’Ema, l’Agenzia europea per i medicinali, ha autorizzato la commercializzazione di Kymriah per il trattamento della leucemia linfoblastica acuta a cellule B nei pazienti pediatrici e fino ai 25 anni di età e per il linfoma diffuso a grandi cellule B negli adulti.
LA CURA DISPONIBILE ANCHE IN ITALIA
Ma l'approvazione di Ema non significa automaticamente accesso garantito a tutti. Tutt'altro. Sino ad oggi i pazienti italiani che necessitavano della terapia potevano ottenerla solo per via compassionevole. Un numero decisamente inferiore (circa 50) rispetto a chi ne ha bisogno, circa 400-600 pazienti all'anno. "In questi ultimi 12 mesi, dopo l’approvazione dell’Ema – spiega Paolo Corradini, Direttore della Divisione di Ematologia della Fondazione IRCCS Istituto Nazionale dei Tumori di Milano– si è creata una grandissima aspettativa nei pazienti e nelle loro famiglie nei confronti di questo trattamento, per cui siamo davvero lieti che AIFA abbia concluso l’iter, arrivando all’approvazione di una delle due molecole commerciali. Si tratta di un grande passo del Paese che si mette in linea con tutte le altre nazioni europee che lo hanno approvato. Siamo quindi riconoscenti di questo sforzo che ha fatto il Ministero della Salute per mettere a disposizione dei cittadini italiani un trattamento così importante, costoso e complesso da gestire”. Da settembre, finalmente, anche i pazienti italiani potranno accedere alle terapia.

Daniele Banfi
Giornalista professionista del Magazine di Fondazione Umberto Veronesi dal 2011. Laureato in Biologia presso l'Università Bicocca di Milano - con specializzazione in Genetica conseguita presso l'Università Diderot di Parigi - ha un master in Comunicazione della Scienza ottenuto presso l'Università La Sapienza di Roma. In questi anni ha seguito i principali congressi mondiali di medicina (ASCO, ESMO, EASL, AASLD, CROI, ESC, ADA, EASD, EHA). Tra le tante tematiche approfondite ha raccontato l’avvento dell’immunoterapia quale nuova modalità per la cura del cancro, la nascita dei nuovi antivirali contro il virus dell’epatite C, la rivoluzione dei trattamenti per l’ictus tramite la chirurgia endovascolare e la nascita delle nuove terapie a lunga durata d’azione per HIV. Dal 2020 ha inoltre contribuito al racconto della pandemia Covid-19 approfondendo in particolare l'iter che ha portato allo sviluppo dei vaccini a mRNA. Collabora con diverse testate nazionali.